 Промежуточные соединения цикла трикарбоновых кислот, покинувшие цикл и задействованные в синтезе различных соединений, замещаются за счёт специальных анаплеротических реакций. Кроме того, ацетил-КоА является также продуктом окисления жирных кислот, так что цикл трикарбоновых кислот участвует и в катаболизме жиров.
Промежуточные соединения цикла трикарбоновых кислот, покинувшие цикл и задействованные в синтезе различных соединений, замещаются за счёт специальных анаплеротических реакций. Кроме того, ацетил-КоА является также продуктом окисления жирных кислот, так что цикл трикарбоновых кислот участвует и в катаболизме жиров.
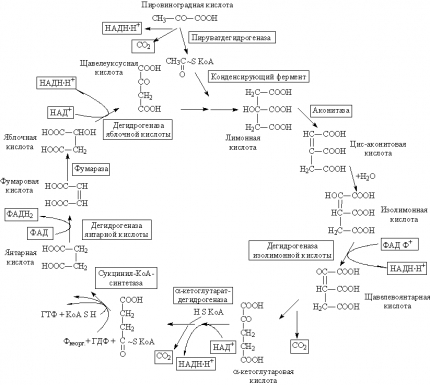
Цитрат затем изомеризуется в изоцитрат (изолимонную кислоту), который далее дегидрируется и декарбоксилируется до пятиуглеродной кислоты — α-кетоглутарата. Кетоглутарат вновь декарбоксилируется, превращаясь в четырёхуглеродный сукцинат (янтарная кислота).
Выше были рассмотрены реакции, составляющие один оборот цикла трикарбоновых кислот
Четыре из восьми стадий цикла представляют собой окислительные процессы, выделяющаяся при этих процессах энергия окисления эффективно запасается в виде восстановленныхкоферментов NADH и FADH2. Хотя цикл трикарбоновых кислот занимает центральное место в энергетическом метаболизме, его роль не сводится к получению и запасанию энергии. Четырёх- и пятиуглеродные промежуточные соединения цикла служат предшественниками для синтеза многих соединений.
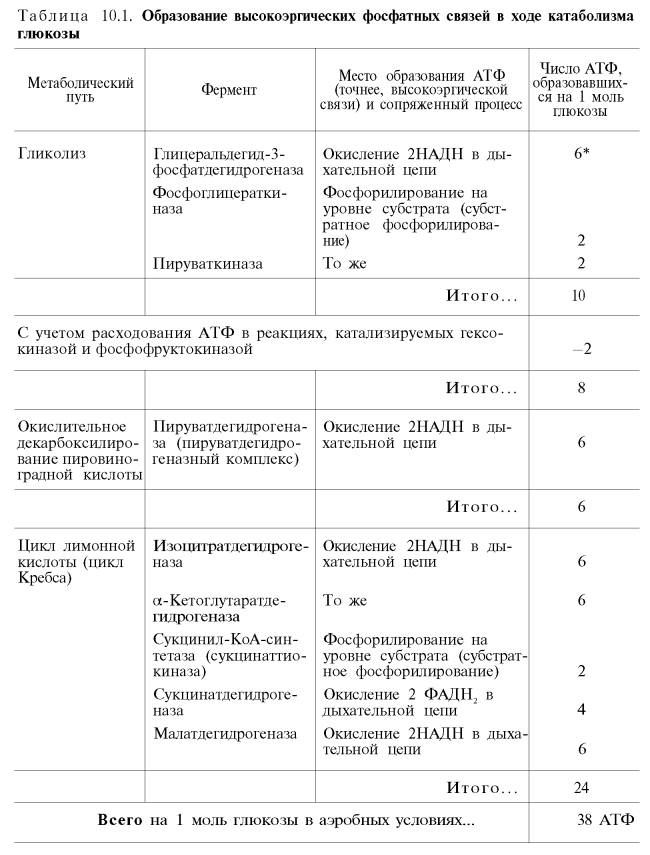
Таким образом, цикл трикарбоновых кислот является амфиболическим путём, он связывает катаболические и анаболические процессы
У большей части бактерий ферменты цикла трикарбоновых кислот находятся в цитозоле, а плазматическая мембрана выполняет функции, аналогичные функциям внутренней мембраны митохондрий. В этой реакции метильная группа в составе ацетильной группы ацетил-СоА присоединяется к карбонильной группе (второму атому углерода, C2-атом) оксалоацетата.
Цитратсинтаза была закристаллизована, и был проведён её рентгеноструктурный анализ в присутствии и отсутствии её субстрата и ингибиторов. В роли кислоты при атаке оксалоацетата выступает другой остаток гистидина, His320, отдающий оксалоацетату свой протон. Тиоэфирная связь в цитроил-СоА гидролизуется с высвобождением СоА и образованием цитрата. Аконитаза содержит железосерный кластер, который служит как для связывания субстрата в активном центре, так и для каталитической гидратации или дегидратации.
Декарбоксилирование оксалосукцината облегчается оттягиванием электронной плотности ионом Mn2+ (или Mg2+). В результате образуется промежуточное енольное соединение. Енольное соединение перестраивается, превращаясь в α-кетоглутарат.
Осуществляемые ими реакции в остальном идентичны. Ферменты E2 обоих комплексов также очень похожи, и оба ковалентно связываются с липоатом. Эта энергозапасающая реакция включает промежуточные этапы, на которых молекула фермента сама становится фосфорилированной по остатку гистидина в активном центре. Этот фермент содержит 3 различных железосерных кластера и одну молекулу ковалентно связанного с ним FAD, являющегося простетической группой фермента.
Однако при приготовлении клеточного экстракта содержимое клеток, в том числе и ферменты, разбавляется в 100 или 1000 раз. Двухуглеродная ацетильная группа входит в цикл, соединясь с оксалоацетатом. Атомы углерода, которые принесены ацетильной группой, могут покидать цикл в виде СО2 только на последующих оборотах цикла.
Доступность субстратов для цитратсинтазы (ацетил-СоА и оксалоацетата) варьирует в зависимости от состояния клетки и иногда сдерживает скорость образования цитрата. NADH, продукт окисления изоцитрата и α-кетоглутарата, при некоторых условиях накапливается, и при большом значении отношения / обе дегидрогеназные реакции строго подавляются.
У эукариот NAD-зависимый изозим локализован в митохондриальном матриксе и участвует в цикле трикарбоновых кислот. Как упоминалось выше, все реакции цикла трикарбоновых кислот происходят в митохондриях, и в митохондриях же располагается дыхательная цепь (на внутренней мембране).


